Đồng, tiếng Anh là Copper, là nguyên tố hóa học trong bảng tuần hoàn nguyên tố có ký hiệu là Cu, có số hiệu nguyên tử bằng 29. Đồng là kim loại dẻo có độ dẫn điện và dẫn nhiệt cao. Đồng nguyên chất mềm và dễ uốn; bề mặt đồng tươi có màu cam đỏ. Nó được sử dụng làm chất dẫn nhiệt và điện, vật liệu xây dựng, và thành phần của các hợp kim của nhiều kim loại khác nhau.
Đồng là một trong số ít các kim loại xuất hiện trong tự nhiên ở dạng kim loại có thể sử dụng trực tiếp thay vì khai thác từ quặng. Do đó, nó được con người sử dụng từ rất sớm khoảng 8000 TCN. Nó là kim loại đầu tiên được nung chảy từ quặng của nó vào khoảng 5000 TCN, kim loại đầu tiên được đúc thành khối vào khoảng 4000 TCN và kim loại đầu tiên được tạo thành hợp kim với các loại khác, là thiếc để tạo ra đồng điếu vào khoảng 3500 TCN.[4]
Bạn đang đọc: Đồng – Wikipedia tiếng Việt
Kim loại và các hợp kim của nó đã được sử dụng cách đây hàng ngàn năm. Trong thời kỳ La Mã, đồng chủ yếu được khai thác ở Síp, vì thế tên gọi ban đầu của kim loại này là сyprium (kim loại Síp), sau đó được gọi tắt là сuprum.[5] Các hợp chất của nó thường tồn tại ở dạng muối đồng(II), chúng thường có màu xanh lam hoặc xanh lục của các loại khoáng như ngọc lam và trong lịch sử đã được sử dụng rộng rãi làm chất nhuộm. Các công trình kiến trúc được xây dựng có đồng bị ăn mòn tạo ra màu xanh lục verdigris (hoặc patina).
Các ion đồng ( II ) tan trong nước với nồng độ thấp hoàn toàn có thể dùng làm chất diệt khuẩn, diệt nấm và làm chất dữ gìn và bảo vệ gỗ. Với số lượng đủ lớn, những ion này là chất độc so với những sinh vật bậc cao hơn, với nồng độ thấp hơn, nó là một vi chất dinh dưỡng so với hầu hết những thực vật và động vật hoang dã bậc cao hơn. Nơi tập trung chuyên sâu đồng đa phần trong khung hình động vật hoang dã là gan, cơ và xương. [ 6 ] Cơ thể người trưởng thành chứa khoảng chừng 1,4 đến 2,1 mg đồng trên mỗi kg cân nặng. [ 7 ]
 Đồng ở nhiệt độ nóng chảy cao hơn điểm nóng chảy của nó một chút ít làm cho nó có ánh hồng khi đủ ánh sáng sẽ làm cho nó rạng rỡ hơn với màu cam đỏ .Đồng, bạc và vàng đều nằm trong nhóm 11 của bảng tuần hoàn nên chúng có nhiều thuộc tính giống nhau : chúng có 1 electron trong phân lớp s1 nằm trước nhóm d10 và được đặc trưng bởi tính dẻo và dẫn điện cao. Các orbital được lấp đầy những electron trong những nguyên tố này không góp phần nhiều vào những tương tác nội nguyên tử, đa phần ảnh hưởng tác động bởi những electron phân lớp s trải qua những link sắt kẽm kim loại. Trái ngược với những sắt kẽm kim loại mà phân lớp d không được lấp đầu bởi những electron, những link sắt kẽm kim loại trong đồng thiếu những đặc thù của link cộng hóa trị và chúng tương đối yếu. Điều này lý giải tại sao những tinh thể đồng riêng không liên quan gì đến nhau có độ dẻo cao và độ cứng thấp. [ 8 ] Ở quy mô lớn, việc thêm vào những khuyết tật trong ô mạng tinh thể như ranh giới hạt, sẽ làm cản trở dòng vật tư dưới áp lực đè nén nén từ đó làm tăng độ cứng của nó. Ví dụ, đồng thường được đưa ra thị trường ở dạng polycrystalline hạt mịn, dạng này có độ cứng lớn hơn dạng monocrystalline. [ 9 ]Độ cứng thấp của đồng giúp lý giải một phần tính dẫn điện cao của nó ( 59.6 × 106 S / m ) và cũng như tính dẫn nhiệt cao, những đặc thù này được xếp hạng thứ 2 trong số những sắt kẽm kim loại nguyên chất có đặc thù tương tự như ở nhiệt độ phòng. [ 10 ] ( trong số những sắt kẽm kim loại nguyên chất ở nhiệt độ phòng chỉ có bạc có độ dẫn điện cao hơn ). Đặc điểm này là do điện trở suất so với sự luân chuyển electron trong những sắt kẽm kim loại ở nhiệt độ phòng hầu hết bắt nguồn từ sự tán xạ của electron so với xê dịch nhiệt của mạng tinh thể, mà điện trở xuất này tương đối yếu so với cho một sắt kẽm kim loại mềm. [ 8 ] Mật độ dòng thấm tối đa của đồng trong không khí ngoài trời vào khoảng chừng 3,1 × 106 A / m², vượt trên giá trị này nó khởi đầu nóng quá mức. [ 11 ] Cùng với những sắt kẽm kim loại khác, nếu đồng được đặt cạnh sắt kẽm kim loại khác, ăn mòn galvanic sẽ diễn ra. [ 12 ]Cùng với lưu huỳnh và vàng ( cả hai đều có màu vàng ), đồng là một trong 3 nguyên tố có màu tự nhiên khác với màu xám hoặc bạc. [ 13 ] Đồng tinh khiết có màu đỏ cam và tạp ra màu lam ngọc khi tiếp xúc với không khí. Màu đặc trưng này của đồng tạo ra từ sự chuyển tiếp electron giữa phân lớp 3 d và phân lớp 4 s – nguồn năng lượng chênh lệch do sự quy đổi trạng thái electrong giữa hai phân lớp này tương ứng với ánh sáng cam. Cơ chế xảy ra tựa như so với màu vàng của vàng và lưu huỳnh. [ 8 ]
Đồng ở nhiệt độ nóng chảy cao hơn điểm nóng chảy của nó một chút ít làm cho nó có ánh hồng khi đủ ánh sáng sẽ làm cho nó rạng rỡ hơn với màu cam đỏ .Đồng, bạc và vàng đều nằm trong nhóm 11 của bảng tuần hoàn nên chúng có nhiều thuộc tính giống nhau : chúng có 1 electron trong phân lớp s1 nằm trước nhóm d10 và được đặc trưng bởi tính dẻo và dẫn điện cao. Các orbital được lấp đầy những electron trong những nguyên tố này không góp phần nhiều vào những tương tác nội nguyên tử, đa phần ảnh hưởng tác động bởi những electron phân lớp s trải qua những link sắt kẽm kim loại. Trái ngược với những sắt kẽm kim loại mà phân lớp d không được lấp đầu bởi những electron, những link sắt kẽm kim loại trong đồng thiếu những đặc thù của link cộng hóa trị và chúng tương đối yếu. Điều này lý giải tại sao những tinh thể đồng riêng không liên quan gì đến nhau có độ dẻo cao và độ cứng thấp. [ 8 ] Ở quy mô lớn, việc thêm vào những khuyết tật trong ô mạng tinh thể như ranh giới hạt, sẽ làm cản trở dòng vật tư dưới áp lực đè nén nén từ đó làm tăng độ cứng của nó. Ví dụ, đồng thường được đưa ra thị trường ở dạng polycrystalline hạt mịn, dạng này có độ cứng lớn hơn dạng monocrystalline. [ 9 ]Độ cứng thấp của đồng giúp lý giải một phần tính dẫn điện cao của nó ( 59.6 × 106 S / m ) và cũng như tính dẫn nhiệt cao, những đặc thù này được xếp hạng thứ 2 trong số những sắt kẽm kim loại nguyên chất có đặc thù tương tự như ở nhiệt độ phòng. [ 10 ] ( trong số những sắt kẽm kim loại nguyên chất ở nhiệt độ phòng chỉ có bạc có độ dẫn điện cao hơn ). Đặc điểm này là do điện trở suất so với sự luân chuyển electron trong những sắt kẽm kim loại ở nhiệt độ phòng hầu hết bắt nguồn từ sự tán xạ của electron so với xê dịch nhiệt của mạng tinh thể, mà điện trở xuất này tương đối yếu so với cho một sắt kẽm kim loại mềm. [ 8 ] Mật độ dòng thấm tối đa của đồng trong không khí ngoài trời vào khoảng chừng 3,1 × 106 A / m², vượt trên giá trị này nó khởi đầu nóng quá mức. [ 11 ] Cùng với những sắt kẽm kim loại khác, nếu đồng được đặt cạnh sắt kẽm kim loại khác, ăn mòn galvanic sẽ diễn ra. [ 12 ]Cùng với lưu huỳnh và vàng ( cả hai đều có màu vàng ), đồng là một trong 3 nguyên tố có màu tự nhiên khác với màu xám hoặc bạc. [ 13 ] Đồng tinh khiết có màu đỏ cam và tạp ra màu lam ngọc khi tiếp xúc với không khí. Màu đặc trưng này của đồng tạo ra từ sự chuyển tiếp electron giữa phân lớp 3 d và phân lớp 4 s – nguồn năng lượng chênh lệch do sự quy đổi trạng thái electrong giữa hai phân lớp này tương ứng với ánh sáng cam. Cơ chế xảy ra tựa như so với màu vàng của vàng và lưu huỳnh. [ 8 ]

 Tháp Đông của Royal Observatory, Edinburgh. Sự độc lạ giữa đồng được tân trang lại năm 2010 và màu lục nguyên thủy của đồng năm 1894 hoàn toàn có thể thấy được rõ ràng .
Tháp Đông của Royal Observatory, Edinburgh. Sự độc lạ giữa đồng được tân trang lại năm 2010 và màu lục nguyên thủy của đồng năm 1894 hoàn toàn có thể thấy được rõ ràng .
Đồng tạo nhiều hợp chất khác nhau với các trạng thái oxy hóa +1 và +2, mà thường được gọi theo thứ tự là cuprous và cupric.Nó không phản ứng với nước, nhưng phản ứng chậm với oxy trong không khí tạo thành một lớp oxide đồng màu nâu đen. Ngược lại với sự oxy hóa của sắt trong không khí ẩm, lớp oxide này sau đó sẽ ngăn cản sự ăn mòn. Một lớp màu lục của verdigris (Đồng(II) carbonat) thường có thể bắt gặp trên các công trình cổ có sử dụng đồng như Tượng Nữ thần tự do, tượng bằng đồng lớn nhất trên thế giới được xây dựng dùng repoussé and chasing.[14] Hydrogen sulfide và sulfide phản ứng với đồng tạo ra các hợp chất đồng sulfide khác nhau trên bề mặt. Trong trường hợp phản ứng với sulfide, ăn mòn đồng diễn ra khi đồng tiếp xúc với không khí có chứa các hợp chất sulfide.[15] Các dung dịch amoni chứa oxy có thể tạo ra một phức chất hòa tan trong nước với đồng, khi phản ứng với oxy và acid clohydric để tạo thành đồng chloride và hydro peroxide bị acid hóa để tạo thành các muối đồng(II). Đồng(II) chloride và đồng phản ứng với nhau tạo thành đồng(I) chloride.[16]
Đồng có 29 đồng vị. 63C u and 65C u là đồng vị bền, với 63C u chiếm khoảng chừng 69 % đồng xuất hiện trong tự nhiên ; cả hai đều có spin 3/2. [ 17 ] Các đồng vị còn lại có tính phóng xạ, trong đó đồng bị phóng xạ bền nhất là 67C u với chu kỳ luân hồi bán rã 61,83 giờ. [ 17 ] Bảy đồng vị kích thích đặc trưng nhất là 68 mCu sống sót lâu nhất với chu kỳ luân hồi bán rã 3,8 phút. Các đồng vị với số khối lớn hơn 64 phân rã β -, ngược lại những đồng vị có số khối dưới 64 thì phân rã β +. 64C u, có chu kỳ luân hồi bán rã 12,7 giờ, phân rã theo cả hai chính sách trên. [ 18 ]62C u và 64C u có những ứng dụng đáng chú ý quan tâm. 64C u chất được sử dụng trong chụp hình tia-X, và dạng tạo phức với chelate hoàn toàn có thể được dùng trong điều trị ung thư. 62C u được dùng trong 62C u – PTSM là một chiêu thức vết phóng xạ trong chụp cắt lớp bằng positron. [ 19 ]
Đồng hoàn toàn có thể tìm thấy như là đồng tự nhiên hoặc trong dạng khoáng chất. Đồng tự nhiên là một dạng polycrystal, với những tinh thể riêng không liên quan gì đến nhau lớn nhất đã được ghi nhận có size 4,4 × 3,2 × 3,2 cm. [ 20 ] Khối đồng nguyên tố lớn nhất có cân nặng 420 tấn, được tìm thấy năm 1857 trên bán đảo Keweenaw ở Michigan, Hoa Kỳ. [ 21 ] Có nhiều dạng khoáng chứa đồng như cacbonat azurit ( 2C uCO3Cu ( OH ) 2 ) và malachit ( CuCO3Cu ( OH ) 2 ) là những nguồn để sản xuất đồng, cũng như là những sulfide như chalcopyrit ( CuFeS2 ), bornit ( Cu5FeS4 ), covellit ( CuS ), chalcocit ( Cu2S ) và những oxide như cuprit ( Cu2O ) .Phần lớn đồng trích xuất được trong những mỏ lộ thiên trong những tài nguyên có ít hơn 1 % đồng. Các ví dụ gồm có : mỏ Chuquicamata ở Chilê và mỏ El Chino ở New Mexico. Nước Ta có mỏ đồng Sinh Quyền ở Tỉnh Lào Cai .Đồng xuất hiện trong vỏ Trái Đất với hàm lượng 50 ppm, [ 21 ] và hoàn toàn có thể được tổng hợp trong những ngôi sao 5 cánh có khối lượng lớn. [ 22 ]
 Mỏ Chuquicamata ở Chile là một trong những mỏ đồng lộ thiên lớn nhất quốc tế .
Mỏ Chuquicamata ở Chile là một trong những mỏ đồng lộ thiên lớn nhất quốc tế . Xu hướng sản xuất trên quốc tế
Xu hướng sản xuất trên quốc tế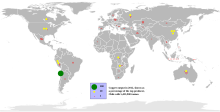 Sản lượng đồng năm 2005
Sản lượng đồng năm 2005 Giá đồng tiến trình 2003 – 2011, USD / tấnHầu hết đồng được khai thác hoặc chiết tách ở dạng đồng sulfide từ những mỏ đồng porphyr khai thác lộ thiên chứa từ 0,4 đến 1,0 % đồng. Ví dụ một số ít mỏ như : mỏ Chuquicamata ở Chile ; Bingham Canyon Mine ở Utah, Hoa Kỳ ; và El Chino Mine ở New Mexico, Hoa Kỳ. Theo Cục Khảo sát địa chất Anh, năm 2005, Chile là nước đứng vị trí số 1 về khai thác đồng chiếm tối thiểu 1/3 sản lượng đồng quốc tế, theo sau là Hoa Kỳ, Indonesia và Peru. [ 10 ] Đồng cũng được tịch thu qua quy trình In-situ leach. Nhiều nơi ở tiểu bang Arizona được xem là những ứng viên cho chiêu thức này. [ 23 ] Lượng đồng đang đượng sử dụng đang tăng và số lượng có sẵn là hầu hết không đủ để cho phép toàn bộ những nước để đạt đến mức độ sử dụng của quốc tế tăng trưởng. [ 24 ]
Giá đồng tiến trình 2003 – 2011, USD / tấnHầu hết đồng được khai thác hoặc chiết tách ở dạng đồng sulfide từ những mỏ đồng porphyr khai thác lộ thiên chứa từ 0,4 đến 1,0 % đồng. Ví dụ một số ít mỏ như : mỏ Chuquicamata ở Chile ; Bingham Canyon Mine ở Utah, Hoa Kỳ ; và El Chino Mine ở New Mexico, Hoa Kỳ. Theo Cục Khảo sát địa chất Anh, năm 2005, Chile là nước đứng vị trí số 1 về khai thác đồng chiếm tối thiểu 1/3 sản lượng đồng quốc tế, theo sau là Hoa Kỳ, Indonesia và Peru. [ 10 ] Đồng cũng được tịch thu qua quy trình In-situ leach. Nhiều nơi ở tiểu bang Arizona được xem là những ứng viên cho chiêu thức này. [ 23 ] Lượng đồng đang đượng sử dụng đang tăng và số lượng có sẵn là hầu hết không đủ để cho phép toàn bộ những nước để đạt đến mức độ sử dụng của quốc tế tăng trưởng. [ 24 ]
Đồng đã được sử dụng tối thiểu là cách nay 10.000 năm, nhưng có hơn 95 % tổng thể đồng đã từng được khai thác và nấu chảy đã được tách chỉ mở màn từ thập niên 1900. Với nhiều nguồn tài nguyên tự nhiên, tổng lượng đồng trên Trái Đất là rất lớn ( khoảng chừng 1014 tấn nằm trong vòng vài km của vỏ Trái Đất, hoặc tương tự 5 triệu năm khai thác với vận tốc khai thác hiện tại. Tuy nhiên, chỉ có một tỷ suất nhỏ trữ lượng này là có giá trị kinh tế tài chính trong điều kiện kèm theo ngân sách và công nghệ tiên tiến hiện tại. Nhiều ước tính trữ lượng đồng hiện tại cho thấy việc khai thác hoàn toàn có thể diễn ra từ 25 đến 60 năm tùy thuộc vào những giả định cốt lõi như vận tốc tăng trưởng. [ 25 ] Tái chế là một nguồn chính của đồng trong quốc tế tân tiến. [ 26 ] Do ảnh hưởng tác động bởi nhiều yếu tố khác nhau, sản lượng và đáp ứng đồng trong tương lai là một chủ đề còn nhiều tranh cãi, gồm có cả khái niệm về đỉnh đồng, tương tự như như đỉnh dầu .Giá đồng trong lịch sử dân tộc là không không thay đổi, [ 27 ] và nó tăng gấp 5 lần từ giá thấp duy trì 60 năm từ US $ 1,32 / kg trong tháng 6 năm 1999 đến US $ 8,27 / kg trong tháng 5 năm 2006. Nó rớt từ US $ 5,29 / kg trong tháng 2 năm 2007, sau đó tăng lên US $ 7,71 / kg tháng 4 năm 2007. [ 28 ] Tháng 2 năm 2009, nhu yếu toàn thế giới giảm và Ngân sách chi tiêu sản phẩm & hàng hóa giảm mạnh từ mức cao của năm trước là US $ 1,51 / lb. [ 29 ]
Hàm lượng đồng trong quặng trung bình chỉ 0,6%, và hầu hết quặng thương mại là các loại đồng sulfide, đặc biệt là chalcopyrit (CuFeS2) và ít hơn là chalcocit (Cu2S).[30] Các khoáng này được tách ra từ các quặng được nghiền để nâng hàm lượng lên 10–15% đồng bằng froth flotation hay bioleaching.[31] Nung vật liệu này với silica trong flash smelting để loại sắt ở dạng xỉ. Quá trình này khai thác dễ dàng chuyển sắt sulfide thành dạng oxide của nó, sau đó các oxide này phản ứng với silica để tạo ra xỉ silicat nổi lên trên khối nóng chảy. Sản phẩm tạo ra copper matte chứa Cu2S sau đó được roasted để chuyển tất cả các sulfide thành oxide:[30]
- 2 Cu2S + 3 O2 → 2 Cu2O + 2 SO2
Oxide đồng được chuyển thành đồng blister theo phản ứng nung:
- 2 Cu2O → 4 Cu + O2
Quá trình Sudbury matte chỉ biến đổi 1/2 sulfide thành oxide và sau đó sử dụng oxide này để loại phần sulfide còn lại thành oxide. Sản phẩm này sau đó đem điện phân.
This step exploits the relatively easy reduction of copper oxides to copper metal. Khí thiên nhiên được thổ qua blister để loại hầu hết oxy còn lại và áp dụng tinh chế điện (electrorefining) để tạo ra đồng tinh khiết:[32]
- Cu2+ + 2 e– → Cu
Đồng, giống như nhôm, hoàn toàn có thể tái chế 100 % mà không bị giảm chất lượng mặc dầu ở dạng thô hoặc nằm trong những loại sản phẩm khác. Về khối lượng, đồng là sắt kẽm kim loại được tái chế thông dụng xếp hàng thứ 3 sau sắt và nhôm. Ước tính có khoảng chừng 80 % đồng đã từng được khai thác hiện tại vẫn còn sử dụng. [ 33 ] Theo Metal Stocks in Society report của International Resource Panel, phân chia trung bình đầu người về đồng hiện đang sử dụng trong xã hội là 35 – 55 kg. Phần nhiều trong số này là ở những nước tăng trưởng nhiều ( 140 – 300 kg / người ) hơn là những nước ít tăng trưởng ( 30 – 40 kg / người ) .Quá trình tái chế đồng tuân theo những bước gần như tương tự như với chiết tách đồng nhưng yên cầu ít quy trình hơn. Đồng phế liệu có độ tinh khiết cao được nung trong lò cao và sau đó được khử và đúc thành billet và ingot ; những phế liệu có độ tinh khiết thấp hơn được tinh chế bằng mạ điện trong một bể acid sulfuric. [ 34 ]
Mục Lục
Thời đại đồ đồng đá[sửa|sửa mã nguồn]
Đồng Open trong tự nhiên ở dạng đồng sắt kẽm kim loại và đã được ghi chép trong những tư liệu của một số ít nền văn minh cổ đại, và nó có lịch sử vẻ vang sử dụng tối thiểu là 9.000 năm TCN ở Trung Đông [ 35 ]. Hoa tai bằng đồng đã được tìm thấy ở miền bắc Iraq có niên đại 8.700 năm TCN [ 36 ]. Có dẫn chứng cho thấy rằng vàng và sắt thiên thạch ( không phải sắt nung chảy ) là những sắt kẽm kim loại duy nhất vào thời đó mà con người đã sử dụng trước khi Open đồng. [ 37 ] Lịch sử nấu đồng được cho là theo những quy trình sau : 1 ) làm cứng nguội đồng tự sinh, 2 ) Ủ luyện, 3 ) nung chảy, và 4 ) đúc mẫu chảy. Ở miền đông nam Anatolia, cả bốn kỹ thuật này đều Open trong khoảng chừng đầu của thời đại đồ đá mới khoảng chừng 7500 TCN. [ 38 ]Chỉ khi nông nghiệp được ý tưởng động lập ở nhiều nơi trên quốc tế, đồng nung chảy cũng được ý tưởng ở nhiều nơi khác nhau. Có lẽ đồng được phát hiện ở Trung Quốc trước 2800 TCN, ở Trung Mỹ vào khoảng chừng năm 600, và Đông Phi vào khoảng chừng thế kỷ IX hay X. [ 39 ] Đúc mẫu chảy được ý tưởng năm 4500 – 4000 TCN ở Khu vực Đông Nam Á [ 35 ] và việc định tuổi cacbon đã được triển khai ở một mỏ tại Alderley Edge, Cheshire, Vương Quốc Anh cho tuổi 2280 – 1890 TCN. [ 40 ] Người băng Ötzi, người đàn ông được định tuổi vào thời gian 3300 – 3200 TCN, được phát hiện có bọc sáp với đồng ở phần đầu đồng có đô tinh khiết 99,7 % ; làm lượng asen cao trong tóc nên người ta cho rằng ông có tương quan đến việc nấu chảy đồng. [ 41 ] Các thí nghiệm với đồng tương hỗ với việc phát hiện ra những sắt kẽm kim loại khác ; đặc biệt quan trọng, đồng nấu chảy làm phát hiện ra nấu chảy sắt. [ 41 ] Việc sản xuất đồng trong xã hội Old Copper Complex ở Michigan và Wisconsin được xác lập tuổi khoảng chừng 6000 đến 3000 TCN. [ 42 ] [ 43 ]
Thời đại đồ đồng[sửa|sửa mã nguồn]
Việc sử dụng đồng đỏ đã phát triển trong thời đại của các nền văn minh được đặt tên là thời đại đồ đồng hay thời đại đồng đỏ. Thời kỳ quá độ trong các khu vực nhất định giữa thời kỳ đồ đá mới và thời kỳ đồ sắt được đặt tên là thời kỳ đồ đồng, với một số công cụ bằng đồng có độ tinh khiết cao được sử dụng song song với các công cụ bằng đá. Đồ đồng của nền văn minh Vinča có tuổi 4500 TCN.[44] Người ta còn tìm thấy các đồ vật bằng đồng nguyên chất và đồng đỏ ở các thành phố Sumeria có niên đại 3.000 năm TCN, và các đồ vật cổ đại của người Ai Cập bằng đồng và hợp kim của đồng với thiếc cũng có niên đại tương tự[45]
Thời đại đồ đồng đã khởi đầu ở Đông Nam châu Âu vào tầm 3700 – 3300 TCN, ổ Tây Bắc châu Âu khoảng chừng 2500 TCN. Nó kết thúc khi mở màn thời đại đồ sắt khoảng chừng 2000 – 1000 TCN ở vùng Cận Đông, và 600 TCN ở Bắc Âu. Sự chuyển tiếp giữa thời đại đồ đá mới và đồ đồng trước đây từng được gọi là thời kỳ đồ đồng đá, khi những công cụ bằng đồng được dùng cùng lúc với công cụ đồ đá. Thuật ngữ này dần bị giảm đi ở vài nơi trên quốc tế, thời đại đồng đá và thời đại đá mới đều kết thúc cùng lúc. Đồng thau, một kim loại tổng hợp của đồng với kẽm, được biết đến từ thời kỳ Hy Lạp nhưng chỉ được sử dụng thoáng rộng bởi người La Mã. [ 45 ]
Giống những tiếng Đông phương khác, nguồn gốc từ đồng từ Tiếng Trung Quốc 铜 ( bình âm : tóng ). Tiếng Thái xài ทองแดง nghĩa là ‘ vàng đỏ ‘ vì đồng có nhiều đặc thù giống vàng như rất dẻo và không dễ sét .
Trong thời của nền văn minh Hy Lạp, kim loại này được biết với tên gọi chalkos. Trong thời kỳ La Mã, nó được biết với tên aes Cyprium (aes là thuật ngữ Latinh chung để chỉ các hợp kim của đồng như đồng đỏ và các kim loại khác, và bởi vì nó được khai thác nhiều ở Síp). Từ những yếu tố lịch sử này, tên gọi của nó được đơn giản hóa thành Cuprum là tên gọi Latinh của đồng.
Trong thần thoại Hy Lạp – La Mã cũng như trong thuật giả kim, đồng có liên quan đến nữ thần Aphrodite (Vệ Nữ) vì vẻ đẹp rực rỡ của nó, việc sử dụng thời cổ đại của nó trong sản xuất gương, và sự liên hệ của nó với Síp, là quê hương của nữ thần. Trong thuật giả kim, ký hiệu của đồng cũng là ký hiệu cho Sao Kim.
Đồng là vật tư dễ dát mỏng, dễ uốn, có năng lực dẫn điện và dẫn nhiệt tốt, thế cho nên nó được sử dụng một cách thoáng rộng trong sản xuất những mẫu sản phẩm :
Đồ đồng là những sản phẩm làm từ nguyên liệu bằng đồng ví dụ như tượng đồng, tranh đồng, trống đồng, mâm đồng, thau đồng… Từ lâu đồ đồng đã được dùng như là những dụng cụ, đồ vật trang trí trong nhà không thể thiếu của người Việt Nam. Nhất là trong tín ngưỡng, văn hóa dân gian. Từ lâu người Việt đã dùng đồng để làm đồ thờ cúng trong ban thờ gia tiên như: hoành phi câu đối bằng đồng, bộ đồ thờ cúng bằng đồng, đỉnh đồng, lư đồng, hạc đồng…
Đồ đồng mỹ nghệ là những sản phẩm mỹ nghệ làm từ đồng ví dụ như: tượng đồng, tranh đồng, trống đồng… Những sản phẩm mỹ nghệ làm từ đồng luôn được ưa chuộng và rất hay được sử dụng trong nhà nhất là tranh đồng, tượng đồng
Đồ đồng phong thủy là những vật phẩm, linh vật, tượng… làm từ đồng. Đồ đồng phong thủy dùng để trấn trạch, hoặc dùng để thỉnh cầu một nguyện vọng nào đó: hóa cát thành hung, giải thoát tai ương, mong muốn những điều tốt đẹp nhất đến với mình và gia đình mình.
Vai trò sinh học[sửa|sửa mã nguồn]
Đồng là nguyên tố vi lượng rất cần thiết cho các loài động, thực vật bậc cao. Đồng được tìm thấy trong một số loại enzym, bao gồm nhân đồng của cytochrom c oxidas, enzym chứa Cu-Zn superoxid dismutas, và nó là kim loại trung tâm của chất chuyên chở oxy hemocyanin. Máu của cua móng ngựa (cua vua) Limulus polyphemus sử dụng đồng thay vì sắt để chuyên chở oxy.[46]
Theo tiêu chuẩn RDA của Mỹ về đồng so với người lớn khỏe mạnh là 0,9 mg / ngày .Đồng được luân chuyển hầu hết trong máu bởi protein trong huyết tương gọi là ceruloplasmin. Đồng được hấp thụ trong ruột non và được luân chuyển tới gan bằng link với albumin. [ 47 ]Một bệnh gọi là bệnh Wilson sinh ra bởi những khung hình mà đồng bị giữ lại, mà không tiết ra bởi gan vào trong mật. Căn bệnh này, nếu không được điều trị, hoàn toàn có thể dẫn tới những tổn thương não và gan .Người ta cho rằng kẽm và đồng là cạnh tranh đối đầu về phương diện hấp thụ trong cỗ máy tiêu hóa do đó việc nhà hàng dư thừa một chất này sẽ làm thiếu vắng chất kia .Các điều tra và nghiên cứu cũng cho thấy 1 số ít người mắc bệnh về thần kinh như bệnh schizophrenia có nồng độ đồng cao hơn trong khung hình. Tuy nhiên, hiện vẫn chưa rõ mối tương quan của đồng với bệnh này như thế nào ( là do khung hình nỗ lực tích góp đồng để chống lại bệnh hay nồng độ cao của đồng là do căn bệnh này gây ra ) .
Có rất nhiều chủng loại kim loại tổng hợp của đồng – Các gương đồng là kim loại tổng hợp của 4 phần đồng với một phần thiếc, đồng thau còn gọi là Latông hay đồng vàng là kim loại tổng hợp của đồng với kẽm, và đồng đỏ hay còn gọi là Burông là kim loại tổng hợp của đồng với thiếc, và hoàn toàn có thể dùng để chỉ bất kể kim loại tổng hợp nào của đồng như đồng điếu nhôm. Đồng là một trong những hợp phần quan trọng nhất của bạc và vàng carat và que hàn carat dùng trong công nghiệp đá quý, kiểm soát và điều chỉnh màu, độ cứng và điểm nóng chảy của những kim loại tổng hợp được tạo ra. [ 48 ] Các loại que hàn không chì gồm có kẽm tạo kim loại tổng hợp với một lượng nhỏ đồng và những sắt kẽm kim loại khác. [ 49 ]
Hợp kim của đồng với nickel được gọi là đồng niken, được sử dụng làm đồng tiền mệnh giá thấp ở dạng áo bên ngoài. Đồng 5-cent Mỹ (hiện được gọi là nickel) chứa 75% đồng và 25% nickel ở dạng đồng nhất. Hợp kim gồm 90% đồng và 10% nickel, có độ chống ăn mòn đáng chú ý, được dùng trong nhiều ứng dụng có tiếp xúc với nước biển, tuy nhiên nó dễ bị ăn mòn do các hợp chất sulfide tồn tại trong các cảng và cửa sông bị ô nhiễm.[50] Các hợp kim của đồng với nhôm (khoảng 7%) có màu vàng nhạt và được dùng trong trang trí.[21] Shakudō là một hợp kim đồng được dùng làm trang trí ở Nhật chứa một tỉ lệ thấp vàng, khoảng 4–10%, nó có thể bị gỉ tạo ra màu xanh đậm hoặc màu đen.[51]
Các trạng thái oxy hóa chung của đồng gồm có trạng thái đồng ( I ) ít không thay đổi Cu + 1 ; và trạng thái không thay đổi hơn đồng ( II ), Cu + 2, [ 52 ] chúng tạo thành những muối có màu lam hoặc lục-lam. Dưới những điều kiện kèm theo không thông thường, trạng thái Cu + 3 hoàn toàn có thể được tạo ra .
Các hợp chất hai cấu tử[sửa|sửa mã nguồn]
Khi phối hợp với những nguyên tố khác, những hợp chất đơn thuần nhất của đồng là loại hai cấu tử, tức gồm có chỉ hai nguyên tố như những oxide, sulfide, và halide. Dạng oxide sống sót ở loại đồng ( I ) và đồng ( II ), tựa như loại sulfide gồm đồng ( I ) sulfide và đồng ( II ) sulfide .Các muối đồng ( I ) với halogen ( gồm đồng ( I ) fluoride, đồng ( I ) chloride, đồng ( I ) bromide, và đồng ( I ) iodide ) cũng sống sót, trong đồng ( II ) gồm đồng ( II ) fluoride, đồng ( II ) chloride, đồng ( II ) bromide và đồng ( II ) iodide. Tuy vậy, có những người đã tìm cách để điều chế đồng ( II ) iodide nhưng chỉ tạo ra đồng ( I ) iodide và iod. [ 52 ]
- 2 Cu2+ + 4 I− → 2 CuI + I2
 Đồng ( II ) tạo ra màu xanh lam đậm với sự xuất hiện của chất link ammoniac. Chất tạo màu ở đây là Đồng ( II ) sulfat tetraminĐồng có năng lực tạo ra phức chất. Trong dung dịch lỏng, đồng ( II ) sống sót ở dạng [ Cu ( H2O ) 6 ] 2 +. Phức này biểu lộ vận tốc trao đổi với nước nhanh nhất ( vận tốc những chất link và tách link với nước ) trong bất kể phức nước-kim loại chuyển tiếp. Khi thêm dung dịch natri hydroxide vào sẽ tạo kết tủa chất rắn đồng ( II ) hydroxide có màu lam nhạt. Phương trình đơn thuần là :
Đồng ( II ) tạo ra màu xanh lam đậm với sự xuất hiện của chất link ammoniac. Chất tạo màu ở đây là Đồng ( II ) sulfat tetraminĐồng có năng lực tạo ra phức chất. Trong dung dịch lỏng, đồng ( II ) sống sót ở dạng [ Cu ( H2O ) 6 ] 2 +. Phức này biểu lộ vận tốc trao đổi với nước nhanh nhất ( vận tốc những chất link và tách link với nước ) trong bất kể phức nước-kim loại chuyển tiếp. Khi thêm dung dịch natri hydroxide vào sẽ tạo kết tủa chất rắn đồng ( II ) hydroxide có màu lam nhạt. Phương trình đơn thuần là : Sơ đồ Pourbaix của đồng trong thiên nhiên và môi trường không tạo phức ( chỉ chăm sóc đến những ion khác OH – ). Nồng độ ion 0,001 m ( mol / kg water ). Nhiệt độ 25 °C .
Sơ đồ Pourbaix của đồng trong thiên nhiên và môi trường không tạo phức ( chỉ chăm sóc đến những ion khác OH – ). Nồng độ ion 0,001 m ( mol / kg water ). Nhiệt độ 25 °C .
- Cu2+ + 2 OH− → Cu(OH)2
Dung dịch amonia cũng tạo kết tủa tựa như. Khi thêm lượng amonia dư, kết tủa này tan tạo thành tetramin đồng ( II ) :
- Cu(H2O)4(OH)2 + 4 NH3 → [Cu(H2O)2(NH3)4]2+ + 2 H2O + 2 OH−
Nhiều oxyanion khác tạo thành những phức như đồng ( II ) axetat, đồng ( II ) nitrat, và đồng ( II ) cacbonat. Đồng ( II ) sunfat tạo những tinh thể pentahydrate màu lam, là hợp chất đồng phổ cập trong phòng thí nghiệm. Nó được dùng để diệt nấm được gọi là Hợp chất Bordeaux. [ 53 ]
 3)4(H2O)2]2+, minh họa cho cấu trúc bát diện phổ biến của đồng(II).Mỏ hình của phức [ Cu ( NH ( HO ), minh họa cho cấu trúc bát diện phổ cập của đồng ( II ) .Polyol là hợp chất chứa nhiều hơn một nhóm chức alcohol, nhìn chung phản ứng với những muốn đồng ( II ). Ví dụ, những muối đồng được dùng để thử chất khử đường. Đặc biệt sử dụng thuốc thử Benedict và dung dịch Fehling có mặt đường được ghi lại bằng màu của nó đổi khác từ xanh lam Cu ( II ) sang đỏ của đồng ( I ) oxide. [ 54 ] Thuốc thử Schweizer và những phức tương quan với ethylenediamine và những amine tan trong cellulose. [ 55 ] Các amino acid tạo thành những phức chelat rất bền với đồng ( II ). Các thử nghiệm hóa-ướt so với những ion đồng sống sót, nó tương quan đến kali ferrocyanua, tạo kết tủa với những muối đồng ( II ) .
3)4(H2O)2]2+, minh họa cho cấu trúc bát diện phổ biến của đồng(II).Mỏ hình của phức [ Cu ( NH ( HO ), minh họa cho cấu trúc bát diện phổ cập của đồng ( II ) .Polyol là hợp chất chứa nhiều hơn một nhóm chức alcohol, nhìn chung phản ứng với những muốn đồng ( II ). Ví dụ, những muối đồng được dùng để thử chất khử đường. Đặc biệt sử dụng thuốc thử Benedict và dung dịch Fehling có mặt đường được ghi lại bằng màu của nó đổi khác từ xanh lam Cu ( II ) sang đỏ của đồng ( I ) oxide. [ 54 ] Thuốc thử Schweizer và những phức tương quan với ethylenediamine và những amine tan trong cellulose. [ 55 ] Các amino acid tạo thành những phức chelat rất bền với đồng ( II ). Các thử nghiệm hóa-ướt so với những ion đồng sống sót, nó tương quan đến kali ferrocyanua, tạo kết tủa với những muối đồng ( II ) .
Hóa đồng hữu cơ[sửa|sửa mã nguồn]
Các hợp chất chứa link cacbon-đồng được gọi là những hợp chất đồng-hữu cơ. Chúng phản ứng mạnh với oxy tạo ra đồng ( I ) oxide và có nhiều ứng dụng trong hóa học. Chúng được tổng hợp bằng cách cho phản ứng giữa những hợp chất đồng ( I ) với thuốc thử Grignard, terminal alkyne hay thuốc thử organolithi ; [ 56 ] đặc biệt quan trọng, phản ứng ở đầu cuối được miêu tả tạo ra thuốc thử Gilman. Các chất này trãi qua những phản ứng thay thế sửa chữa với alkyl halide tạo thành những loại sản phẩm tích hợp ; do đó, chúng có vai trò quan trọng trong nghành nghề dịch vụ tổng hợp hữu cơ. Đồng ( I ) acetylua nhạy sốc cao trong những phản ứng như Cadiod-Chodkiewicz coupling [ 57 ] và Sonogashira coupling. [ 58 ] Conjugate addition vào enone [ 59 ] và carbocupration của những alkyne [ 60 ] cũng hoàn toàn có thể đạt được những hợp chất đồng hữu cơ. Đồng ( I ) tạo ra một loạt những phức yếu với anken và cacbon monoxide, đặc biệt quan trọng xuất hiện của những phức amine. [ 61 ]
Đồng ( III ) thường được tìm thấy ở dạng xác oxide, ví dụ như kali cuprat, KCuO2 là chất rắn màu dương đen. [ 62 ] Các hợp chất đồng ( III ) được điều tra và nghiên cứu thoáng đãng nhất là những chất siêu dẫn cuprat. Đồng ytri bari oxide ( YBa2Cu3O7 ) có cả Cu ( II ) và Cu ( III ) nằm ở TT. Giống như dạng oxide, fluoride là anion base cao [ 63 ] và được dùng làm chất không thay đổi những ion sắt kẽm kim loại ở những trạng thái oxy hóa cao. Cả đồng ( III ) và thậm chí còn đồng ( IV ) fluoride là sống sót theo thứ tự ở dạng K3CuF6 và Cs2CuF6. [ 64 ]Một số protein đồng tạo những phức oxo đặc trưng cho đồng ( III ). [ 65 ] Với những tetrapeptit, một phức đồng ( III ) có màu tía được không thay đổi hóa bởi những chất amit khử proton. [ 66 ]Các phức đồng ( III ) cũng được tìm thấy ở dạng trung gian trong những phản ứng của hợp chất đồng-hữu cơ. [ 67 ]
| NFPA 704 “Biểu đồ cháy” |
|---|
 020 020 |
| Biểu đồ cháy của đồng kim loại |
![]() Wikipedia tiếng Việt không bảo đảm và không chịu trách nhiệm về tính pháp lý và độ chính xác của các thông tin có liên quan đến y học và sức khỏe. Độc giả cần liên hệ và nhận tư vấn từ các bác sĩ hay các chuyên gia. Khuyến cáo cẩn thận khi sử dụng các thông tin này. Xem chi tiết tại Wikipedia:Phủ nhận y khoa và Wikipedia:Phủ nhận về nội dung.về tính pháp lý và độ đúng mực của những thông tin có tương quan đến y học và sức khỏe thể chất. Khuyến cáo cẩn trọng khi sử dụng những thông tin này
Wikipedia tiếng Việt không bảo đảm và không chịu trách nhiệm về tính pháp lý và độ chính xác của các thông tin có liên quan đến y học và sức khỏe. Độc giả cần liên hệ và nhận tư vấn từ các bác sĩ hay các chuyên gia. Khuyến cáo cẩn thận khi sử dụng các thông tin này. Xem chi tiết tại Wikipedia:Phủ nhận y khoa và Wikipedia:Phủ nhận về nội dung.về tính pháp lý và độ đúng mực của những thông tin có tương quan đến y học và sức khỏe thể chất. Khuyến cáo cẩn trọng khi sử dụng những thông tin này
Mọi hợp chất của đồng là những chất độc.[cần dẫn nguồn] Đồng kim loại ở dạng bột là một chất dễ cháy.[cần dẫn nguồn] 30g đồng(II) sunfat có khả năng gây chết người.[cần dẫn nguồn] Đồng trong nước với nồng độ lớn hơn 1 mg/lít có thể tạo vết bẩn trên quần áo hay các đồ vật được giặt giũ trong nước đó. Nồng độ an toàn của đồng trong nước uống đối với con người dao động theo từng nguồn, nhưng có xu hướng nằm trong khoảng 1,5 – 2 mg/l. Mức cao nhất có thể chịu được về đồng theo DRI trong chế độ ăn uống đối với người lớn theo mọi nguồn đều là 10 mg/ngày.[cần dẫn nguồn]
Liên kết ngoài[sửa|sửa mã nguồn]
Source: https://1hanoi.com
Category : Kiến trúc